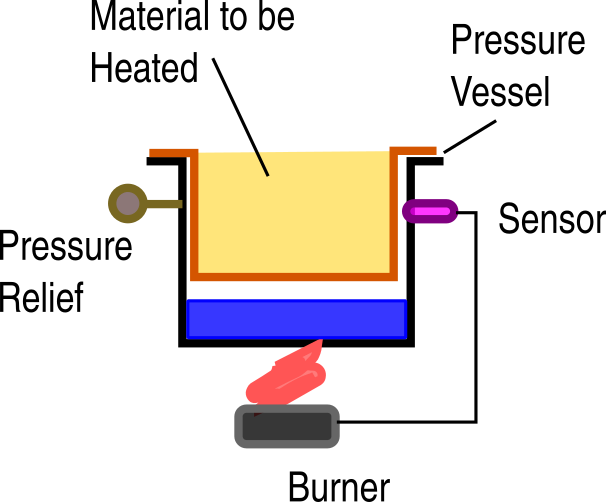
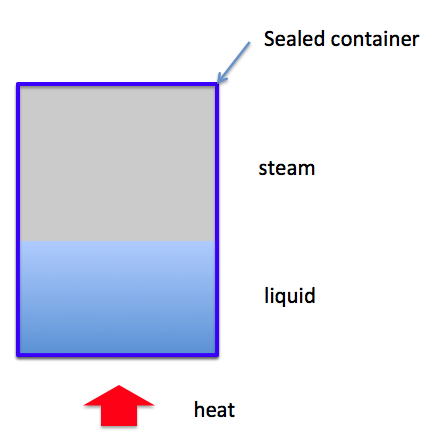
جوشاندن مایع در ظرف دربسته، حرارت کمتری لازم است
ارسال شده: شنبه ۱۴۰۱/۶/۱۹ - ۰۷:۵۶
اگر مایعی را با گرمای نهان L در ظرفی با حجم بی نهایت بجوشانید (یعنی باز به کیهان) حرارت مورد نیاز:
$Q=Lm$
جایی که m جرم مایع جوشانده شده است. با این حال، اگر آن را در ظرفی با حجم محدود V بجوشانید، حرارت مورد نیاز:
$Q=Lm-V\Delta p$
جایی که$ Δp $تغییر فشار است. با چه مکانیزم فیزیکی به سیستم گرمای $VΔp$ به اطراف باز می گردد و چرا؟
اجازه دهید استدلال خود را در پشت فرمول$Q=Lm-V\Delta p$توضیح دهم. طبق تعریف، گرمای نهان تبخیر، تفاوت در آنتالپی بین گاز تبخیر شده و مایع است.
$Lm=H_2-H_1$
اما $H_i=U_i+p_i V$برای i=1,2 بنابراین:$Lm=(U_2+p_2V)-(U_1+p_1V)$$Lm=\Delta U + V\Delta p$و بنابراین:
$\Delta U=Lm-V\Delta p$
در مورد ما هیچ کاری روی سیستم از محیط اطراف انجام نشده است و از این رو تغییر در انرژی داخلی باید صرفاً با افزودن انرژی گرمایی فراهم شود. این بدان معنی است که انرژی گرمایی مورد نیاز برای این تغییر عبارت است از:
$Q=Lm−VΔp$
من فکر می کنم یک مفهوم مرتبط در اینجا وجود دارد که شایان ذکر است. یک سیستم را در $T_1, p_1, V_1$ بگیرید و از طریق یک تغییر برگشت پذیر آن را به حالت $T_2, p_1, V_2$ تغییر دهید. حدس می زنم همه ما موافق باشیم که گرمای تامین شده به سیستم توسط:
$Q=C_p (T_2-T_1)$
اما انرژی درونی توسط:
$dU=dQ−pdV$
بنابراین تغییر انرژی درونی به صورت زیر بدست می آید:
$U=C_p(T_2-T_1)-p_1(V_2-V_1)$
اکنون دوباره از $T_1, p_1, V_1$ شروع می کنیم و در $T_2, p_1, V_2$ به پایان می رسیم (مثلاً با باز کردن یک شیر آب) حجم را از V1 به V2 افزایش می دهیم. سپس برای تغییر دما اقدام کنید زیرا در هیچ مرحله ای روی سیستم کاری انجام نمی شود، گرمای اعمال شده باید برابر با تغییر انرژی داخلی سیستم باشد، یعنی.
$Q_2= C_p(T_2-T_1)-p_1(V_2-V_1)$
البته این دقیقاً همان استدلال بالا است، اما من فکر میکنم استفاده از ظرفیتهای گرمایی آن را به طور مستقیم ساده میکند.I hope I have helped you in understanding the question. Roham hesami, seventh semester
aerospace engineering

$Q=Lm$
جایی که m جرم مایع جوشانده شده است. با این حال، اگر آن را در ظرفی با حجم محدود V بجوشانید، حرارت مورد نیاز:
$Q=Lm-V\Delta p$
جایی که$ Δp $تغییر فشار است. با چه مکانیزم فیزیکی به سیستم گرمای $VΔp$ به اطراف باز می گردد و چرا؟
اجازه دهید استدلال خود را در پشت فرمول$Q=Lm-V\Delta p$توضیح دهم. طبق تعریف، گرمای نهان تبخیر، تفاوت در آنتالپی بین گاز تبخیر شده و مایع است.
$Lm=H_2-H_1$
اما $H_i=U_i+p_i V$برای i=1,2 بنابراین:$Lm=(U_2+p_2V)-(U_1+p_1V)$$Lm=\Delta U + V\Delta p$و بنابراین:
$\Delta U=Lm-V\Delta p$
در مورد ما هیچ کاری روی سیستم از محیط اطراف انجام نشده است و از این رو تغییر در انرژی داخلی باید صرفاً با افزودن انرژی گرمایی فراهم شود. این بدان معنی است که انرژی گرمایی مورد نیاز برای این تغییر عبارت است از:
$Q=Lm−VΔp$
من فکر می کنم یک مفهوم مرتبط در اینجا وجود دارد که شایان ذکر است. یک سیستم را در $T_1, p_1, V_1$ بگیرید و از طریق یک تغییر برگشت پذیر آن را به حالت $T_2, p_1, V_2$ تغییر دهید. حدس می زنم همه ما موافق باشیم که گرمای تامین شده به سیستم توسط:
$Q=C_p (T_2-T_1)$
اما انرژی درونی توسط:
$dU=dQ−pdV$
بنابراین تغییر انرژی درونی به صورت زیر بدست می آید:
$U=C_p(T_2-T_1)-p_1(V_2-V_1)$
اکنون دوباره از $T_1, p_1, V_1$ شروع می کنیم و در $T_2, p_1, V_2$ به پایان می رسیم (مثلاً با باز کردن یک شیر آب) حجم را از V1 به V2 افزایش می دهیم. سپس برای تغییر دما اقدام کنید زیرا در هیچ مرحله ای روی سیستم کاری انجام نمی شود، گرمای اعمال شده باید برابر با تغییر انرژی داخلی سیستم باشد، یعنی.
$Q_2= C_p(T_2-T_1)-p_1(V_2-V_1)$
البته این دقیقاً همان استدلال بالا است، اما من فکر میکنم استفاده از ظرفیتهای گرمایی آن را به طور مستقیم ساده میکند.I hope I have helped you in understanding the question. Roham hesami, seventh semester
aerospace engineering