اگر اتم ها دايره شكل هستند،چه جوري كنار هم قرار گرفتند؟
- جوجه كوچولو
عضویت : سهشنبه ۱۳۸۶/۴/۱۲ - ۱۳:۵۶
پست: 304-
سپاس: 3
تماس:
اگر اتم ها دايره شكل هستند،چه جوري كنار هم قرار گرفتند؟
به نام خدا
سلام دوستان.اين سوال ذهن منو مشغول كرده:
اگر اتم ها دايره شكل هستند،چه جوري كنار هم قرار گرفتند؟يعني بين اونا فضاي خالي وجود داره؟
لطفا جواب بديد.
با تشكر
جوجه كوچولو
سلام دوستان.اين سوال ذهن منو مشغول كرده:
اگر اتم ها دايره شكل هستند،چه جوري كنار هم قرار گرفتند؟يعني بين اونا فضاي خالي وجود داره؟
لطفا جواب بديد.
با تشكر
جوجه كوچولو
اولا دايره اي نه كروي دوما كروي هم نيستند بلكه داراي شكلهاي متفاوت و در حال تغيير اند و بين انها هم فاصله هست اما آنها به طور منظم كنار هم نيستند طبق اصل عدم قطعيت.
انها با نوجه به اوربيتالهاي آخرين لايه شان محتملترين شكل را ي توان براي انها پيش بيني كرد اگر كمي صبر كني در سالهاي دبيرستان مي خواني !
انها با نوجه به اوربيتالهاي آخرين لايه شان محتملترين شكل را ي توان براي انها پيش بيني كرد اگر كمي صبر كني در سالهاي دبيرستان مي خواني !
- جوجه كوچولو
عضویت : سهشنبه ۱۳۸۶/۴/۱۲ - ۱۳:۵۶
پست: 304-
سپاس: 3
تماس:
- جوجه كوچولو
عضویت : سهشنبه ۱۳۸۶/۴/۱۲ - ۱۳:۵۶
پست: 304-
سپاس: 3
تماس:
-
samanta_ict
عضویت : یکشنبه ۱۳۸۵/۴/۴ - ۲۳:۰۰
پست: 814-
سپاس: 6
جوجه كوچولو, ببين اتم ها دايره نيستن .
اتمها از الكترون هايي كه به دور هسته مي گردند تشكيل شده (البته الكترون ها هم ابر هستند يعني با استفاده از يكسري مفاهيم به اسم اوربيتاله ها مي توان جاي دقيق انها را در ابر الكتروني مشخص كرد ي). يعني اون فضايي رو كه مي گن الكترون ها هستن رو مثل يه ابر در نظر مي گيرن كه توش بر اساس يك سري معادلات موجي مي توان احتمال وجود الكترون ها را در قسمت هاي مختلف اين ابر به دست آورد .يعني مثل يه لوله بسته مي مونن (مثل لوله پليكا كه توش رو كسي نمي بينه حالا توي اين لوله پليكا يه دونه توپ كوچولو داره حركت مي كنه ولي ما چون نمي بينيم ميگيم الان بر اساس احتمال فلان جاست يا احتمال داره مسير حركتش اين طوري باشه .
حالا ابر الكتروني هم مثل همون لوله پليكا مي مونه كه توش توپ الكترون حركت مي كنه حالا ما نمي دونيم الكترون كجاست ديگه .پس مي يايم با احتساب ك سري معادلات طول موجي كه در رياضيات عالي مطرح مي شوند احتمال وجود الكترون را در جاي جاي اين ابر الكتروني به دست مي آوريم و اين معادلات را رسم مي كنيم (هر معادله اي رو ميشه رسم كرد تو رياضي 1 دبيرستان نوشته )بعد يك سري شكل به دست ميياد به اسم اوربيتال حالا اون اربيتال ها جاهايي هستن كه توي اون ابر الكتروني از همه جا مساعد تر و احتمال اينكه الكترون داخل اون ها باشه از بقيه جاها بيشتره اين معني اوربيتال بود .
حالا ميگن هر اطراف هر هسته چند لايه ابر الكتروني هست .
خوب حالا يه سوال آيا وقتي دو تا ابر تو آسمون كنار هم قرار مي گيرن بينشون فضاي خالي باقي مي مونه ؟!!!!!!!!!!!!!
كه اين جا باقي بمونه .
اون نظريه رادفورد و بور بود كه اتم را به شكل دايره اي در نظر مي گرفت ولي تيوري جديد اتم ها ابر الكتروني هست .
در كل يعني مثل دو تا ابر مي مونن كه با هم برخورد مي كنن و كنار هم قرار مي گيرن .
خداوكيلي از اين ساده تر نمي تونستم بگم اميدوارن درس كوانتوم بنده ! رو متوجه شده باشيد .
زنگ خورد بفرماييد تو حياط !!!
اتمها از الكترون هايي كه به دور هسته مي گردند تشكيل شده (البته الكترون ها هم ابر هستند يعني با استفاده از يكسري مفاهيم به اسم اوربيتاله ها مي توان جاي دقيق انها را در ابر الكتروني مشخص كرد ي). يعني اون فضايي رو كه مي گن الكترون ها هستن رو مثل يه ابر در نظر مي گيرن كه توش بر اساس يك سري معادلات موجي مي توان احتمال وجود الكترون ها را در قسمت هاي مختلف اين ابر به دست آورد .يعني مثل يه لوله بسته مي مونن (مثل لوله پليكا كه توش رو كسي نمي بينه حالا توي اين لوله پليكا يه دونه توپ كوچولو داره حركت مي كنه ولي ما چون نمي بينيم ميگيم الان بر اساس احتمال فلان جاست يا احتمال داره مسير حركتش اين طوري باشه .
حالا ابر الكتروني هم مثل همون لوله پليكا مي مونه كه توش توپ الكترون حركت مي كنه حالا ما نمي دونيم الكترون كجاست ديگه .پس مي يايم با احتساب ك سري معادلات طول موجي كه در رياضيات عالي مطرح مي شوند احتمال وجود الكترون را در جاي جاي اين ابر الكتروني به دست مي آوريم و اين معادلات را رسم مي كنيم (هر معادله اي رو ميشه رسم كرد تو رياضي 1 دبيرستان نوشته )بعد يك سري شكل به دست ميياد به اسم اوربيتال حالا اون اربيتال ها جاهايي هستن كه توي اون ابر الكتروني از همه جا مساعد تر و احتمال اينكه الكترون داخل اون ها باشه از بقيه جاها بيشتره اين معني اوربيتال بود .
حالا ميگن هر اطراف هر هسته چند لايه ابر الكتروني هست .
خوب حالا يه سوال آيا وقتي دو تا ابر تو آسمون كنار هم قرار مي گيرن بينشون فضاي خالي باقي مي مونه ؟!!!!!!!!!!!!!
كه اين جا باقي بمونه .
اون نظريه رادفورد و بور بود كه اتم را به شكل دايره اي در نظر مي گرفت ولي تيوري جديد اتم ها ابر الكتروني هست .
در كل يعني مثل دو تا ابر مي مونن كه با هم برخورد مي كنن و كنار هم قرار مي گيرن .
خداوكيلي از اين ساده تر نمي تونستم بگم اميدوارن درس كوانتوم بنده ! رو متوجه شده باشيد .
زنگ خورد بفرماييد تو حياط !!!
-
samanta_ict
عضویت : یکشنبه ۱۳۸۵/۴/۴ - ۲۳:۰۰
پست: 814-
سپاس: 6
-
samanta_ict
عضویت : یکشنبه ۱۳۸۵/۴/۴ - ۲۳:۰۰
پست: 814-
سپاس: 6
-
samanta_ict
عضویت : یکشنبه ۱۳۸۵/۴/۴ - ۲۳:۰۰
پست: 814-
سپاس: 6
جوجه كوچولو, شايد نفهمي ولي بد نيست بخونيش
٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬
یکی از برنامه های تحقیقاتی که در حال حاضر در جریان است مطالعه پدیده مکانیک کوانتوم و ماهیت ذرات بنیادین کوچک تر از اتم و همچنین پیدا کردن ارتباط آن با اتم های تشکیل دهنده سلول های مغزی و هوشمندی انسان است. هاینرنبرگ برای اولین بار در اویل قرن بیستم اصل عدم قطعیت را مطرح کرد. وی و همکارانش با استفاده از وسائل آن روز از جمله شتاب دهنده الکترون در یک اختلاف پتانسیل بسیار قوی به این موضوع پی بردند که اتم یک هسته متمرکز دارد ولی الکترون به صورت یک ذره متمرکز دور هسته نمی چرخد. اگر الکترون یک ذره متمرکز با جرم و بار الکتریکی مشخص بود نمی توانست به تنهائی
360
درجه فضائی را پر کند. در صورت نزدیک شدن دو اتم به یکدیگر آنها به هم برخورد می کردند و به هم می چسبیدند. آنها موضوع را به این صورت توجیه کردند که الکترون به صورت جرم متمرکز نیست بلکه به صورت ابر الکترونی است که فضای
360
درجه اتم را با چرخش خود پر کرده و نمی گذارند که اتم ها به هم بچسبند. چرخش مانع از آن می شود که ابر الکترونی اتم به فضای خالی بین ابر الکترونی و هسته مجاور وارد شود. هایزبرگ ثابت کرد که ذرات تشکیل دهنده ابر الکترونی از لحاظ موقعیت مکانی و سرعت وضعیت مشخصی ندارند یعنی در یک لحظه در یک جا هستند و هیج جا نیستند. این موضوع اساس نظریه عدم قطعیت می باشد. حال سئوال اینجاست که آیا روزی به کمک فنآوری نانو می توانیم رابطه بین ذرات بنیادین وتشکیل دهنده الکترون و پروتون را با هوشمندی انسان کشف کنیم؟ یعنی همانطور که امروزه می توانیم اطلاعات را در سیلیکون و نیمه هادی ها ذخیره کنیم، آیا می توانیم در آینده در سلولهای زنده نیز چنین کاری انجام دهیم؟
اگر روزی انسان به این توانائی برسد دیگر حتی دیوار خانه هم هوشمند خواهد بود زیرا فرق بین دیوار، میز و اشیاء با بدن انسان و سلولهای زنده در چیدمان اتمی آنهاست. در نتیجه اگر چیدمان اتم ها و ذرات بنیادین تحت کنترل انسان باشد دنیای فیزیکی کاملا در تسخیر ما خواهد شد
٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬٬
یکی از برنامه های تحقیقاتی که در حال حاضر در جریان است مطالعه پدیده مکانیک کوانتوم و ماهیت ذرات بنیادین کوچک تر از اتم و همچنین پیدا کردن ارتباط آن با اتم های تشکیل دهنده سلول های مغزی و هوشمندی انسان است. هاینرنبرگ برای اولین بار در اویل قرن بیستم اصل عدم قطعیت را مطرح کرد. وی و همکارانش با استفاده از وسائل آن روز از جمله شتاب دهنده الکترون در یک اختلاف پتانسیل بسیار قوی به این موضوع پی بردند که اتم یک هسته متمرکز دارد ولی الکترون به صورت یک ذره متمرکز دور هسته نمی چرخد. اگر الکترون یک ذره متمرکز با جرم و بار الکتریکی مشخص بود نمی توانست به تنهائی
360
درجه فضائی را پر کند. در صورت نزدیک شدن دو اتم به یکدیگر آنها به هم برخورد می کردند و به هم می چسبیدند. آنها موضوع را به این صورت توجیه کردند که الکترون به صورت جرم متمرکز نیست بلکه به صورت ابر الکترونی است که فضای
360
درجه اتم را با چرخش خود پر کرده و نمی گذارند که اتم ها به هم بچسبند. چرخش مانع از آن می شود که ابر الکترونی اتم به فضای خالی بین ابر الکترونی و هسته مجاور وارد شود. هایزبرگ ثابت کرد که ذرات تشکیل دهنده ابر الکترونی از لحاظ موقعیت مکانی و سرعت وضعیت مشخصی ندارند یعنی در یک لحظه در یک جا هستند و هیج جا نیستند. این موضوع اساس نظریه عدم قطعیت می باشد. حال سئوال اینجاست که آیا روزی به کمک فنآوری نانو می توانیم رابطه بین ذرات بنیادین وتشکیل دهنده الکترون و پروتون را با هوشمندی انسان کشف کنیم؟ یعنی همانطور که امروزه می توانیم اطلاعات را در سیلیکون و نیمه هادی ها ذخیره کنیم، آیا می توانیم در آینده در سلولهای زنده نیز چنین کاری انجام دهیم؟
اگر روزی انسان به این توانائی برسد دیگر حتی دیوار خانه هم هوشمند خواهد بود زیرا فرق بین دیوار، میز و اشیاء با بدن انسان و سلولهای زنده در چیدمان اتمی آنهاست. در نتیجه اگر چیدمان اتم ها و ذرات بنیادین تحت کنترل انسان باشد دنیای فیزیکی کاملا در تسخیر ما خواهد شد
-
samanta_ict
عضویت : یکشنبه ۱۳۸۵/۴/۴ - ۲۳:۰۰
پست: 814-
سپاس: 6
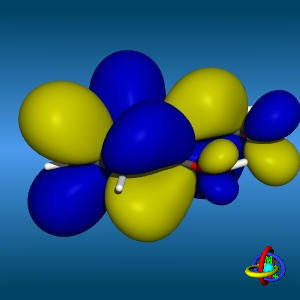
اينم يه توضيح كلي راجع به اوربيتال
از نظر لغوی ، اوربیتال به معنای خانه الکترون میباشد و ناحیهای است که احتمال یافتن الکترون در آن زیاد است. معادله شرودینگر پایه مکانیک موجی است. این معادله بر حسب یک تابع موجی (ψ) برای الکترون نوشته میشود. از حل معادله شرودینگر اتم هیدروژن یک سلسله جواب به عنوان تابع موج بدست میآید. تابع موج ناحیهای در اطراف هسته را نشان میدهد که در آن ناحیه ، احتمال یافتن الکترون وجود دارد. تابع موجی یک الکترون ، آنچه را که اوربیتال نامیده میشود، توصیف میکند
مقدمه
اوربیتال محدودهای از فضای اطراف هسته میباشد که احتمال یافتن الکترون در آن وجود دارد. این احتمال در نزدیکی هسته بیشترین مقدار را دارد. ولی برای تمام نقاطی از فضا که فاصله معینی از هسته دارند، احتمال معینی وجود دارد. هر اوربیتال میتواند حداکثر دو الکترون را در خود جای دهد. دو الکترونی که در یک اوربیتال جای میگیرند، دارای اسپین مخالف هستند.
هر الکترون را میتوان با چهار عدد کوانتومی مشخص کرد که به منزله شناسنامه الکترون هستند و فاصله نسبی الکترون از هسته (n) ، لایه فرعی و شکل اوربیتال (L) ، جهت گیری اوربیتال در فضا (s) را بیان میکنند. بر اساس اصل طرد پاولی در یک اتم هیچ دو الکترونی را نمیتوان یافت که تمام چهار عدد کوانتومی آنها یکسان باشد.
تاریخچه
در مورد ساختمان اتم و نحوه قرار گرفتن الکترونها و پروتونها در آن بررسیهای زیادی توسط دانشمندان انجام شده و نظریههای مختلفی ارائه شده است. تامسون اتم را به شکل کرهای یکنواخت از بارهای مثبت تا شعاع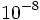 تصور میکرد که بارهای منفی در محیط خارجی کره پراکندهاند. رادرفورد در سال 1911 با استفاده از ذرات آلفا دلایل قانع کنندهای مبنی بر وجود هسته اتم ارائه داد. او اتم را بصورت کره ای تصور میکرد که هسته در وسط آن قرار دارد و الکترونها به فواصل نسبی بینهایت زیاد در خارج از هسته قرار دارند. نیلز بوهر در سال 1913 نظریه ساختمان الکترونی اتم را پیشنهاد کرد.
تصور میکرد که بارهای منفی در محیط خارجی کره پراکندهاند. رادرفورد در سال 1911 با استفاده از ذرات آلفا دلایل قانع کنندهای مبنی بر وجود هسته اتم ارائه داد. او اتم را بصورت کره ای تصور میکرد که هسته در وسط آن قرار دارد و الکترونها به فواصل نسبی بینهایت زیاد در خارج از هسته قرار دارند. نیلز بوهر در سال 1913 نظریه ساختمان الکترونی اتم را پیشنهاد کرد.
این نظریه بر اساس مدل اتمی رادرفورد ، نظریه کوانتومی پلانک و دادههای تجربی حاصل از مطالعه طیفهای اتمی قرار داشت، و بیان میکرد که الکترون اتم هیدروژن فقط میتواند در مدارهای کروی معین (مدارها یا ترازهای انرژی) که بطور متحدالمرکز دور هسته قرار دارند، وجود داشته باشد. این مدارها تابع محدودیت کوانتومی است. شرودینگر در سال 1926 با طرح معادلهای که در آن محدودیت کوانتومی انرژی الکترون و تصور الکترون بصورت موج ساکن ، با هم تلفیق شده بود، تابع موجی الکترون (ψ) را معرفی کرد که مختصات مکان الکترون در فضایی که الکترون در آن یافت میشود و انرژی الکترون از لحاظ ریاضی را به هم مربوط کرد.
اگر الکترون را بصورت ذرهای در حال حرکت به دور هسته در نظر بگیریم، ψ2 متناسب با احتمال یافتن الکترون در جزو معینی از فضاست و احتمال یافتن الکترون در ناحیهای که ابر الکترونی غلیظتر باشد بیشتر است.
تفسیر مکانیکی اوربیتال
شدت هر موج با مجذور دامنه آن متناسب است. تابع موجی (ψ) ، تابع دامنه است. مجذور دامنه یا مجذور تابع موجی برای یک حجم کوچک در هر موقعیتی از فضا با چگالی بار الکترونی در آن حجم متناسب است. میتوان تصور کرد که بار الکترونی به سبب حرکت سریع الکترون بصورت ابر باردار در فضای دور هسته گسترده شده است. این ابر در برخی نواحی غلیظتر از برخی نواحی دیگر است.
احتمال یافتن الکترون در هر ناحیه معین متناسب با چگالی ابر الکترونی در آن ناحیه است. این احتمال در ناحیهای که ابر الکترونی غلیظتر باشد، بیشتر خواهد بود. این تفسیر کوششی برای توصیف مسیر الکترون به عمل نمیآورد، بلکه فقط پیشبینی میکند که احتمال یافتن الکترون در کجا بیشتر است.
از نظر مکانیک کوانتومی هیچ محدودیتی برای وجود الکترون در فضا اطراف هسته وجود ندارد. پس بینهایت اوربیتال وجود دارد.
اعداد کوانتومی
مکانیک موجی که نظریه شرودینگر اساس آن میباشد با استفاده از چهار عدد کوانتومی وضعیت الکترون را توصیف میکند. این اعداد عبارتند از :
عدد کوانتومی اصلی
این عدد نشاندهنده ترازهای انرژی است که الکترونها در آن ترازها به دور هسته گردش میکنند و عدد صحیحی میباشد. این عدد میتواند کلیه مقادیر اعداد صحیح مثبت به استثنای صفر را قبول کند.
عدد کوانتومی اندازه حرکت زاویهای مداری
آرنولد زمر فیلد در سال 1916 پیشنهاد کرد که هر مدار بوهر (n) با شرط n>1 از لایههایی فرعی با اختلاف انرژی کم تشکیل شدهاست. به هر لایه فرعی یک عدد کوانتومی (L) نسبت داده میشود. این عدد نشان دهنده شکل هندسی توزیع تابع احتمال پیدا کردن الکترون در فضای اطراف هسته میباشد وکلیه مقادیر L=0,1,2, … , n-1 را اختیار کند.
عدد کوانتومی مغناطیسی مداری
تعداد اوربیتالهای یک تراز فرعی را میتوان از این عدد استنتاج کرد که در اثر میدان مغناطیسی هر تراز L به این ترازها شکافته میشود. بعنوان مثال میدان مغناطیسی بر اوربیتال کروی S که با عدد L=0 مشخص میشود، تاثیری ندارد چون S تقارن کروی دارد و در تمام جهتها بطور یکسان تحت تاثیر خطوط نیرو قرار میگیرد. این عدد که با m نشان داده می شود، مقادیر ممکن این عدد عبارتند از :
m=+L,…,0,…,-L
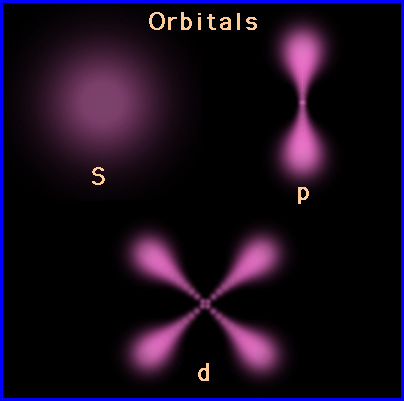
عدد کوانتومی مغناطیسی اسپینی
این عدد مشخص کننده حرکت تقدیمی الکترون است و با نشان داده میشود و میتواند مقادیر 2/1+ , 2/1- را اختیار کند.
ابر الکترونی و مکان الکترون
در مورد یک الکترون در حالت n=1 هیدروژن ، ابر باردار بالاترین چگالی را در نزدیکی هسته دارد و بتدریج که فاصله از هسته افزایش مییابد، رقیقتر میشود. احتمال یافتن الکترون در حجم کوچکی از فضا ، در نزدیکی هسته ، بیشترین مقدار را دارد و با افزایش فاصله از هسته به سمت صفر میل میکند.
لایههای کروی بسیار نازکی را که یکی پس از دیگری بطور متحدالمرکز به دور هسته قرار دارند، تصور کنید. احتمال یافتن الکترون در واحد حجم فضای نزدیک به هسته بیشترین مقدار خود را دارد. ولی در عوض یک لایه نزدیک به هسته ، در مقایسه با لایههای دورتر ، تعداد کمتری واحد حجم را در بر میگیرد. احتمال شعاعی هر دو این عوامل را با هم به حساب میآورد.
نمودار سطح مرزی
احتمال یافتن الکترون در تمام نقاطی که از هسته به فاصله برابر مقداری است که از طریق نظریه بور برای شعاع لایه n=1 تعیین شده است. در نظریه بوهر ، فاصلهای است که همواره الکترون لایه n=1 از هسته دارا است. در مکانیک موجی فاصلهای از هسته است که الکترون در آن حضور بیشتری دارد.
از آنجا که اصولا در هر فاصله معین از هسته ، الکترون امکان حضور دارد، ترسیم ناحیهای با مرز مشخص که احتمال 100 درصد وجود الکترون را در بر بگیرد، ناممکن است. اما میتوان سطح مرزی را ترسیم کرد که بتواند نقاط با احتمال یکسان را به هم بپیوندد و در برگیرنده حجمی باشد که در آن ، احتمال یافتن الکترون زیاد و مثلا در حدود 90 درصد است. چنین شکلی که نمودار سطح مرزی نامیده میشود، برای الکترون اتم هیدروژن در حالت n=1 بصورت کروی میباشد.
انواع اوربیتال
اوربیتال S
اوربیتالهای S دارای تقارن کروی میباشد، تراز n=1 حداکثر دارای دو الکترون است. بنابراین تراز فرعی 1S و 2S و 3S و... هم تقارن کروی دارند، با این تفاوت که اندازه آنها بزرگتر از اوربیتال 1S میباشد.
اوربیتال p
اوربیتال p از سه اوربیتال فرعی تشکیل شده است. هر اوربیتال p به شکل دو کره تغییر شکل یافته است که میتوان آنها را در امتداد یکی از محورهای سه گانه مختصات (z,y,x) تصور کرد از این رو اوربیتالهای p را با مشخص میکنند که در سه جهت مختلف قرار گرفتهاند. اوربیتالهای p از لحاظ انرژی برابرند و در غیاب میدان مغناطیسی نمیتوان تفاوتی بین الکترونهایی که این اوربیتالها را اشغال کردهاند قایل شد. ولی در بررسیهای طیفی که تحت تاثیر یک میدان مغناطیسی قرار میگیرند، هر اوربیتال p به سه خط شکافته میشوند.
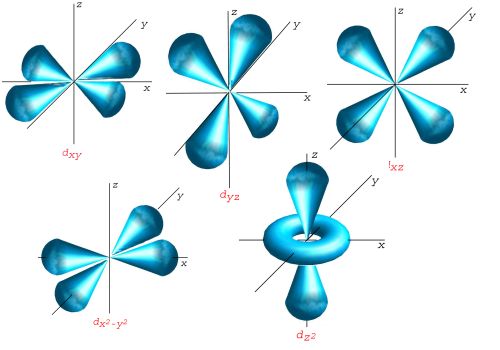
از نظر لغوی ، اوربیتال به معنای خانه الکترون میباشد و ناحیهای است که احتمال یافتن الکترون در آن زیاد است. معادله شرودینگر پایه مکانیک موجی است. این معادله بر حسب یک تابع موجی (ψ) برای الکترون نوشته میشود. از حل معادله شرودینگر اتم هیدروژن یک سلسله جواب به عنوان تابع موج بدست میآید. تابع موج ناحیهای در اطراف هسته را نشان میدهد که در آن ناحیه ، احتمال یافتن الکترون وجود دارد. تابع موجی یک الکترون ، آنچه را که اوربیتال نامیده میشود، توصیف میکند

مقدمه
اوربیتال محدودهای از فضای اطراف هسته میباشد که احتمال یافتن الکترون در آن وجود دارد. این احتمال در نزدیکی هسته بیشترین مقدار را دارد. ولی برای تمام نقاطی از فضا که فاصله معینی از هسته دارند، احتمال معینی وجود دارد. هر اوربیتال میتواند حداکثر دو الکترون را در خود جای دهد. دو الکترونی که در یک اوربیتال جای میگیرند، دارای اسپین مخالف هستند.
هر الکترون را میتوان با چهار عدد کوانتومی مشخص کرد که به منزله شناسنامه الکترون هستند و فاصله نسبی الکترون از هسته (n) ، لایه فرعی و شکل اوربیتال (L) ، جهت گیری اوربیتال در فضا (s) را بیان میکنند. بر اساس اصل طرد پاولی در یک اتم هیچ دو الکترونی را نمیتوان یافت که تمام چهار عدد کوانتومی آنها یکسان باشد.
تاریخچه
در مورد ساختمان اتم و نحوه قرار گرفتن الکترونها و پروتونها در آن بررسیهای زیادی توسط دانشمندان انجام شده و نظریههای مختلفی ارائه شده است. تامسون اتم را به شکل کرهای یکنواخت از بارهای مثبت تا شعاع
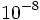 تصور میکرد که بارهای منفی در محیط خارجی کره پراکندهاند. رادرفورد در سال 1911 با استفاده از ذرات آلفا دلایل قانع کنندهای مبنی بر وجود هسته اتم ارائه داد. او اتم را بصورت کره ای تصور میکرد که هسته در وسط آن قرار دارد و الکترونها به فواصل نسبی بینهایت زیاد در خارج از هسته قرار دارند. نیلز بوهر در سال 1913 نظریه ساختمان الکترونی اتم را پیشنهاد کرد.
تصور میکرد که بارهای منفی در محیط خارجی کره پراکندهاند. رادرفورد در سال 1911 با استفاده از ذرات آلفا دلایل قانع کنندهای مبنی بر وجود هسته اتم ارائه داد. او اتم را بصورت کره ای تصور میکرد که هسته در وسط آن قرار دارد و الکترونها به فواصل نسبی بینهایت زیاد در خارج از هسته قرار دارند. نیلز بوهر در سال 1913 نظریه ساختمان الکترونی اتم را پیشنهاد کرد.این نظریه بر اساس مدل اتمی رادرفورد ، نظریه کوانتومی پلانک و دادههای تجربی حاصل از مطالعه طیفهای اتمی قرار داشت، و بیان میکرد که الکترون اتم هیدروژن فقط میتواند در مدارهای کروی معین (مدارها یا ترازهای انرژی) که بطور متحدالمرکز دور هسته قرار دارند، وجود داشته باشد. این مدارها تابع محدودیت کوانتومی است. شرودینگر در سال 1926 با طرح معادلهای که در آن محدودیت کوانتومی انرژی الکترون و تصور الکترون بصورت موج ساکن ، با هم تلفیق شده بود، تابع موجی الکترون (ψ) را معرفی کرد که مختصات مکان الکترون در فضایی که الکترون در آن یافت میشود و انرژی الکترون از لحاظ ریاضی را به هم مربوط کرد.
اگر الکترون را بصورت ذرهای در حال حرکت به دور هسته در نظر بگیریم، ψ2 متناسب با احتمال یافتن الکترون در جزو معینی از فضاست و احتمال یافتن الکترون در ناحیهای که ابر الکترونی غلیظتر باشد بیشتر است.
تفسیر مکانیکی اوربیتال
شدت هر موج با مجذور دامنه آن متناسب است. تابع موجی (ψ) ، تابع دامنه است. مجذور دامنه یا مجذور تابع موجی برای یک حجم کوچک در هر موقعیتی از فضا با چگالی بار الکترونی در آن حجم متناسب است. میتوان تصور کرد که بار الکترونی به سبب حرکت سریع الکترون بصورت ابر باردار در فضای دور هسته گسترده شده است. این ابر در برخی نواحی غلیظتر از برخی نواحی دیگر است.
احتمال یافتن الکترون در هر ناحیه معین متناسب با چگالی ابر الکترونی در آن ناحیه است. این احتمال در ناحیهای که ابر الکترونی غلیظتر باشد، بیشتر خواهد بود. این تفسیر کوششی برای توصیف مسیر الکترون به عمل نمیآورد، بلکه فقط پیشبینی میکند که احتمال یافتن الکترون در کجا بیشتر است.
از نظر مکانیک کوانتومی هیچ محدودیتی برای وجود الکترون در فضا اطراف هسته وجود ندارد. پس بینهایت اوربیتال وجود دارد.
اعداد کوانتومی
مکانیک موجی که نظریه شرودینگر اساس آن میباشد با استفاده از چهار عدد کوانتومی وضعیت الکترون را توصیف میکند. این اعداد عبارتند از :
عدد کوانتومی اصلی
این عدد نشاندهنده ترازهای انرژی است که الکترونها در آن ترازها به دور هسته گردش میکنند و عدد صحیحی میباشد. این عدد میتواند کلیه مقادیر اعداد صحیح مثبت به استثنای صفر را قبول کند.
عدد کوانتومی اندازه حرکت زاویهای مداری
آرنولد زمر فیلد در سال 1916 پیشنهاد کرد که هر مدار بوهر (n) با شرط n>1 از لایههایی فرعی با اختلاف انرژی کم تشکیل شدهاست. به هر لایه فرعی یک عدد کوانتومی (L) نسبت داده میشود. این عدد نشان دهنده شکل هندسی توزیع تابع احتمال پیدا کردن الکترون در فضای اطراف هسته میباشد وکلیه مقادیر L=0,1,2, … , n-1 را اختیار کند.
عدد کوانتومی مغناطیسی مداری
تعداد اوربیتالهای یک تراز فرعی را میتوان از این عدد استنتاج کرد که در اثر میدان مغناطیسی هر تراز L به این ترازها شکافته میشود. بعنوان مثال میدان مغناطیسی بر اوربیتال کروی S که با عدد L=0 مشخص میشود، تاثیری ندارد چون S تقارن کروی دارد و در تمام جهتها بطور یکسان تحت تاثیر خطوط نیرو قرار میگیرد. این عدد که با m نشان داده می شود، مقادیر ممکن این عدد عبارتند از :
m=+L,…,0,…,-L

عدد کوانتومی مغناطیسی اسپینی
این عدد مشخص کننده حرکت تقدیمی الکترون است و با نشان داده میشود و میتواند مقادیر 2/1+ , 2/1- را اختیار کند.
ابر الکترونی و مکان الکترون
در مورد یک الکترون در حالت n=1 هیدروژن ، ابر باردار بالاترین چگالی را در نزدیکی هسته دارد و بتدریج که فاصله از هسته افزایش مییابد، رقیقتر میشود. احتمال یافتن الکترون در حجم کوچکی از فضا ، در نزدیکی هسته ، بیشترین مقدار را دارد و با افزایش فاصله از هسته به سمت صفر میل میکند.
لایههای کروی بسیار نازکی را که یکی پس از دیگری بطور متحدالمرکز به دور هسته قرار دارند، تصور کنید. احتمال یافتن الکترون در واحد حجم فضای نزدیک به هسته بیشترین مقدار خود را دارد. ولی در عوض یک لایه نزدیک به هسته ، در مقایسه با لایههای دورتر ، تعداد کمتری واحد حجم را در بر میگیرد. احتمال شعاعی هر دو این عوامل را با هم به حساب میآورد.
نمودار سطح مرزی
احتمال یافتن الکترون در تمام نقاطی که از هسته به فاصله برابر مقداری است که از طریق نظریه بور برای شعاع لایه n=1 تعیین شده است. در نظریه بوهر ، فاصلهای است که همواره الکترون لایه n=1 از هسته دارا است. در مکانیک موجی فاصلهای از هسته است که الکترون در آن حضور بیشتری دارد.
از آنجا که اصولا در هر فاصله معین از هسته ، الکترون امکان حضور دارد، ترسیم ناحیهای با مرز مشخص که احتمال 100 درصد وجود الکترون را در بر بگیرد، ناممکن است. اما میتوان سطح مرزی را ترسیم کرد که بتواند نقاط با احتمال یکسان را به هم بپیوندد و در برگیرنده حجمی باشد که در آن ، احتمال یافتن الکترون زیاد و مثلا در حدود 90 درصد است. چنین شکلی که نمودار سطح مرزی نامیده میشود، برای الکترون اتم هیدروژن در حالت n=1 بصورت کروی میباشد.
انواع اوربیتال
اوربیتال S
اوربیتالهای S دارای تقارن کروی میباشد، تراز n=1 حداکثر دارای دو الکترون است. بنابراین تراز فرعی 1S و 2S و 3S و... هم تقارن کروی دارند، با این تفاوت که اندازه آنها بزرگتر از اوربیتال 1S میباشد.
اوربیتال p
اوربیتال p از سه اوربیتال فرعی تشکیل شده است. هر اوربیتال p به شکل دو کره تغییر شکل یافته است که میتوان آنها را در امتداد یکی از محورهای سه گانه مختصات (z,y,x) تصور کرد از این رو اوربیتالهای p را با مشخص میکنند که در سه جهت مختلف قرار گرفتهاند. اوربیتالهای p از لحاظ انرژی برابرند و در غیاب میدان مغناطیسی نمیتوان تفاوتی بین الکترونهایی که این اوربیتالها را اشغال کردهاند قایل شد. ولی در بررسیهای طیفی که تحت تاثیر یک میدان مغناطیسی قرار میگیرند، هر اوربیتال p به سه خط شکافته میشوند.

-
samanta_ict
عضویت : یکشنبه ۱۳۸۵/۴/۴ - ۲۳:۰۰
پست: 814-
سپاس: 6
edwardfurlong, استاد فعلا ما براي تفهيم اين دوست به اين نقيضه (!!) پناه برديم .
توكل بر خدا شما هم تز خود را بفرماييد ما هم استفاده ببريم/!
ابته خارج از شوخي edwardfurlong, عزيز اين مباحث جاي خيلي زيادي واسه بحث و اشكال داره ولي آخه اصل اينه كه اگه اشكال گرفتي بتوني جوابشم بدي .
مثلا منم روي اين قضيه شك دارم به دلايل زير :
فضاي بين ابر الكتروني تا هسته آيا خلا 100٪ است .
آيا زماني كه دو ابر الكتروني با هم همپوشي مي كند آيا چگالي الكتروني آن الكترون افزايش نمي يابد و ..
آيا فضاي بين اتم ها در فضاهاي بسيار دور از هم خالي است و ...........
حالا هي يره خواستي نقضش كني به ما هم بوگو.
توكل بر خدا شما هم تز خود را بفرماييد ما هم استفاده ببريم/!
ابته خارج از شوخي edwardfurlong, عزيز اين مباحث جاي خيلي زيادي واسه بحث و اشكال داره ولي آخه اصل اينه كه اگه اشكال گرفتي بتوني جوابشم بدي .
مثلا منم روي اين قضيه شك دارم به دلايل زير :
فضاي بين ابر الكتروني تا هسته آيا خلا 100٪ است .
آيا زماني كه دو ابر الكتروني با هم همپوشي مي كند آيا چگالي الكتروني آن الكترون افزايش نمي يابد و ..
آيا فضاي بين اتم ها در فضاهاي بسيار دور از هم خالي است و ...........
حالا هي يره خواستي نقضش كني به ما هم بوگو.
Re: اگر اتم ها دايره شكل هستند،چه جوري كنار هم قرار گرفتند؟
اتم ها شكل یكسان و مرز روشنی ندارند،جوجه كوچولو نوشته شده:به نام خدا
سلام دوستان.اين سوال ذهن منو مشغول كرده:
اگر اتم ها دايره شكل هستند،چه جوري كنار هم قرار گرفتند؟يعني بين اونا فضاي خالي وجود داره؟
لطفا جواب بديد.
با تشكر
جوجه كوچولو
سیال مانند ابر هستند چون از ابر الكترونی
( و هسته) درست شده اند . این است كه
زمانی هم كه بهم میچسبند، این ابرهای
الكترونی شان هم باهم آمیخته و یك ابر
الكترونی به فورم و شكل دیگری كه
همه این هسته ها را بپوشاند بخود
میگیرند و دیگر " فضای " تهی میان
آنها نمیماند .درست مانند وصل شدن
دو تكه ابر و یا دو قطره آب بهم دیگر.
فیزیك كوانتومی هم شكل احتمالاتی
این ابر ها را بما نشان میدهد.
اگر این را بفهمید دیگر به این گفتار های
"رسمی" و كپی های آورده شده نیازی ندارید.
•



خرد، زنده ی جــاودانی شنــاس
خرد، مايه ی زنــدگانی شنــاس
چنان دان هر آنكس كه دارد خرد
بــدانــش روان را هــمی پــرورد
خرد، مايه ی زنــدگانی شنــاس
چنان دان هر آنكس كه دارد خرد
بــدانــش روان را هــمی پــرورد





